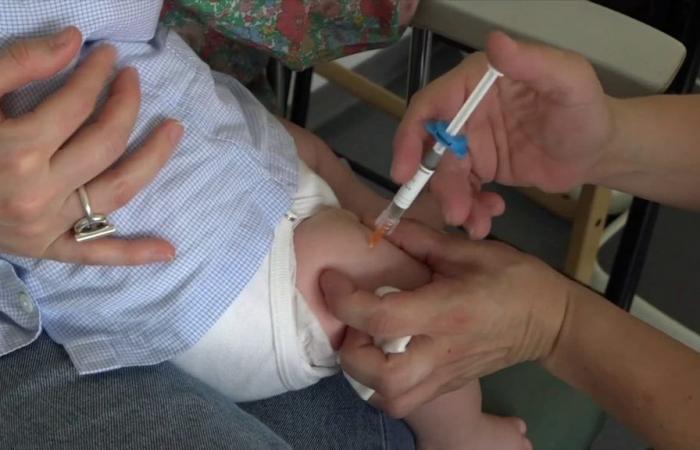
Die wenigen Fälle, die den für die Pharmakovigilanz zuständigen Behörden gemeldet wurden, betrafen größtenteils eine verminderte Wirksamkeit von Beyfortus, wie die National Medicines Safety Agency in einem Folgebericht von diesem Montag, dem 30. September, angibt.
Laut ihrer am Montag veröffentlichten ersten Bewertung der Überwachung von Nebenwirkungen hat die Arzneimittelbehörde (ANSM) keinen „besonderen Risikofaktor“ bei Beyfortus festgestellt, einer auf Antikörpern gegen Bronchiolitis bei Säuglingen basierenden Behandlung, die Eltern von Neugeborenen ein Jahr lang angeboten wird.
Zwischen dem 11. September 2023 und dem 30. April 2024 wurden 244.495 Dosen Beyfortus an Entbindungsstationen und in der Stadt abgegeben, und in diesem Zeitraum wurden 198 Pharmakovigilanz-Fälle gemeldet, darunter 153 als „schwerwiegend“, wie die ANSM in einer Mitteilung am angab die erste vorbeugende Impfkampagne 2023/2024.
Nur 198 Fälle von mehr als 240.000 Dosen
„Die überwiegende Mehrheit (74,7 %) der 198 in der Pharmakovigilanz gemeldeten Fälle berichten von einer geringeren Wirksamkeit oder Unwirksamkeit von Beyfortus mit dem Auftreten einer RSV-Bronchiolitis bei Kindern, die den Antikörper erhielten“, erklärte die Agentur ausführlich.
„Bei diesen Kindern, die nach der Verabreichung von Beyfortus an Bronchiolitis unterschiedlicher Schwere (kein Tod) erkrankten, wurde kein besonderer Risikofaktor festgestellt“, fügte sie hinzu.
Die ANSM erwähnt in ihrem Pharmakovigilanzbericht auch „drei Fälle von plötzlichem Tod“, ohne dass ein ursächlicher Zusammenhang mit Beyfortus nachgewiesen werden konnte. Im ersten Fall „bleiben (…) Zweifel an einer möglichen Verbindung mit Beyfortus bestehen, selbst wenn Risikofaktoren für einen plötzlichen Tod identifiziert wurden“, stellt sie fest.
Im zweiten Fall sei „eine direkte Wirkung von Beyfortus sehr unwahrscheinlich, da die Wirkung 79 Tage nach der Injektion eintritt“, im letzten Fall „ist die Chronologie kaum mit der Zurechenbarkeit von Beyfortus vereinbar“, was jedoch nicht ausgeschlossen werden kann.
Nirsevimab, so der Name des aktiven Moleküls, ist kein Impfstoff, auch wenn er injizierbar ist, sondern eine vorbeugende Behandlung, die verhindert, dass das Hauptvirus, das Bronchiolitis verursacht, das Respiratory Syncytial Virus (RSV), den Organismus infiziert.
„Es wurden Fälle von Atemwegserkrankungen und systemischen Wirkungen nach der Injektion (wie Grippesyndrom, verminderter Appetit, verminderter Muskeltonus) gemeldet, die alle einen günstigen Ausgang hatten“, gab die ANSM außerdem an. Sie stellte fest, dass „ebenfalls ein Einzelfall eines Schlaganfalls gemeldet wurde“, stellte jedoch klar, dass „zum jetzigen Zeitpunkt der kausale Zusammenhang zwischen Beyfortus und diesen Auswirkungen nicht nachgewiesen wurde“. Insgesamt wurden „21 bemerkenswerte Fälle“ gemeldet.
Insgesamt „bestätigen diese Ergebnisse sowie die durchgeführten Studien zur Wirksamkeit das positive Nutzen-Risiko-Verhältnis von Beyfortus gegen Bronchiolitis“, urteilte die Agentur.